Jak budować agentów AI w środowiskach regulowanych GxP
Źródło: Link

Źródło: Link
Vivomeal — działający produkt zbudowany na AI. Przykład tego, co wyjdzie po kursie.
Jeśli pracujesz w branży farmaceutycznej czy medycznej, wiesz doskonale: wdrożenie każdego nowego systemu IT to maraton przez regulacyjne przeszkody. A teraz chcesz wprowadzić agentów AI – systemy, które uczą się i zmieniają w czasie. To przypomina misja niemożliwa? AWS właśnie opublikował praktyczny przewodnik, który pokazuje, jak to zrobić bez łamania zasad GxP.
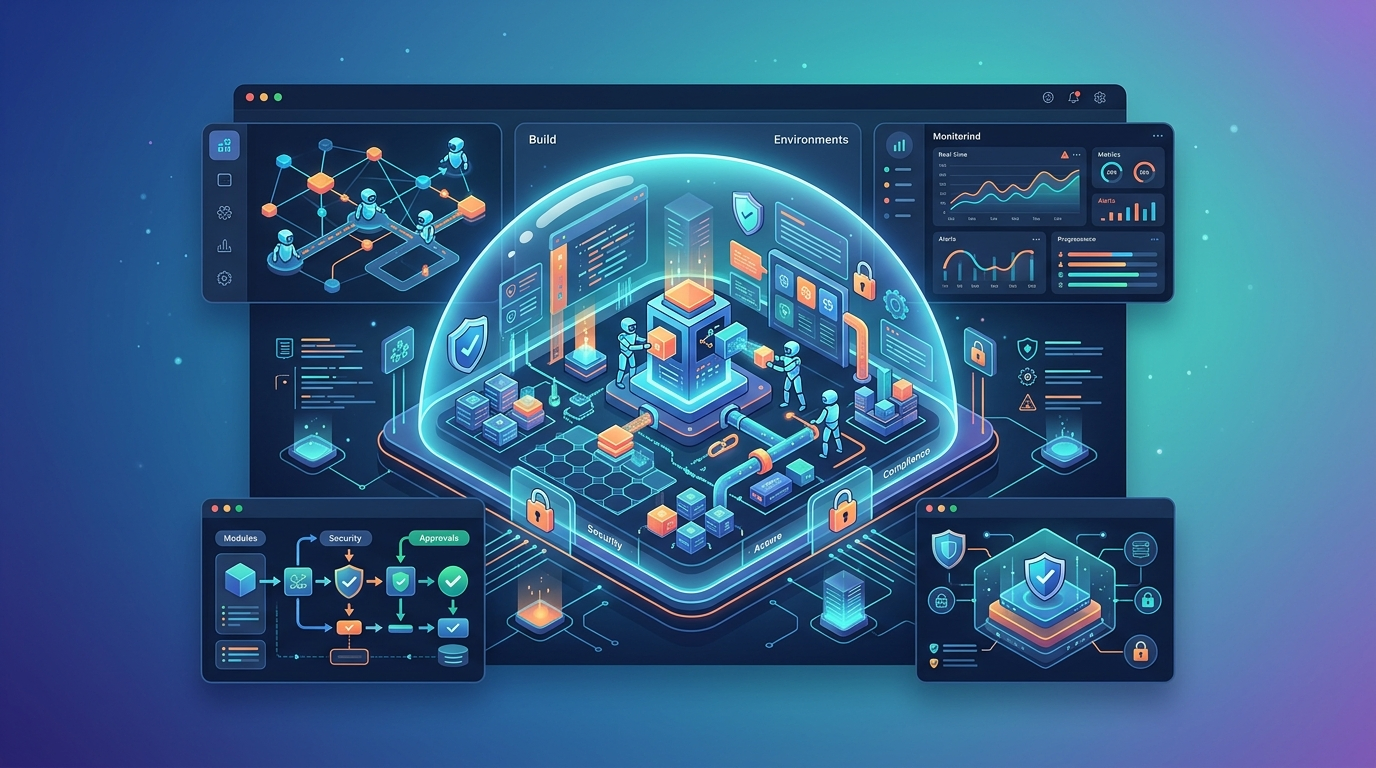
Środowiska GxP (Good Practice) obejmują wszystkie obszary przemysłu regulowanego. Od produkcji leków (GMP) przez badania kliniczne (GCP) po laboratoria (GLP). Tradycyjnie każdy system komputerowy przechodzi przez sztywną walidację CSV, która zakłada jedno: oprogramowanie działa zawsze tak samo. Problem? Agenci AI z definicji są dynamiczni i adaptacyjni.
AWS proponuje przejście z klasycznego Computer System Validation na nowsze podejście Computer Software Assurance. Różnica jest fundamentalna. Zamiast walidować każdą funkcję z osobna, CSA koncentruje się na ocenie ryzyka i zapewnieniu jakości tam, gdzie rzeczywiście ma to znaczenie dla bezpieczeństwa pacjenta i integralności danych.
CSA umożliwia elastyczne podejście do walidacji agentów AI. Zamiast traktować wszystkie komponenty jednakowo, możesz skupić zasoby na krytycznych elementach systemu. Model AI używany do analizy dokumentacji może wymagać innego poziomu kontroli niż agent odpowiedzialny za decyzje dotyczące dawkowania leków (co brzmi całkiem rozsądnie).
AWS przedstawia konkretną architekturę opartą na Amazon Bedrock – platformie, która pozwala budować agentów AI z wbudowanymi mechanizmami kontroli. Kluczowe elementy to:
Szczególnie interesujące jest podejście do zarządzania promptami. W środowisku GxP każdy prompt używany przez agenta AI powinien być wersjonowany i walidowany. Tak, nawet te kilka zdań instrukcji dla modelu. AWS proponuje traktować prompty jak kod – z kontrolą wersji, testami i procedurą zatwierdzania zmian.
Przewodnik AWS nie jest teoretycznym traktatem – pokazuje konkretne przypadki użycia. Agenci AI mogą automatyzować przeglądanie dokumentacji regulacyjnej, wspierać farmakokowigilancję czy przyspieszać analizę danych klinicznych. Wszystko przy zachowaniu zgodności z FDA 21 CFR Part 11 i europejskimi wytycznymi EMA.
Największą wartością tego podejścia jest możliwość iteracyjnego wdrażania AI. Zamiast czekać miesiącami na pełną walidację, możesz uruchomić agenta w trybie asystenta (z nadzorem człowieka), zbierać dane o jego działaniu i stopniowo zwiększać autonomię. To zmienia ekonomię projektów AI w branżach regulowanych – z wieloletnich inwestycji na projekty z wymiernym ROI w perspektywie kwartałów.
Przeczytaj też:
Podoba Ci się ten artykuł?
Co piątek wysyłam podsumowanie najlepszych artykułów tygodnia. Zapisz się!
90 minut praktycznej wiedzy o AI. Pokaze Ci krok po kroku, jak zaczac oszczedzac 10 godzin tygodniowo dzieki sztucznej inteligencji.
Zapisz sie na webinar